Chi phí nghiên cứu và phát triển (R&D) ngày càng tăng, hiện đã vượt quá 3,5 tỷ USD cho mỗi thuốc mới (novel drug), phản ánh sự suy giảm hiệu quả R&D dược phẩm trong suốt năm thập kỷ qua. Mặc dù các báo cáo gần đây cho thấy khả năng xoay chuyển tình thế, bài đánh giá này cung cấp một phân tích ở cấp độ hệ thống nhằm khám phá xem đây là một sự thay đổi về mặt cấu trúc hay chỉ là sự đảo ngược tạm thời. Chúng tôi đã phân tích dữ liệu tài chính từ 200 công ty dược phẩm lớn nhất, các phê duyệt thuốc mới và hơn 80.000 thử nghiệm lâm sàng từ năm 2012 đến 2023. Phân tích của chúng tôi tiết lộ rằng bất chấp sự ổn định gần đây, ngành dược phẩm tiếp tục đối mặt với nhiều thách thức, đặc biệt là do tỷ lệ hao hụt lâm sàng (clinical attrition) tăng cao ở giai đoạn muộn, cho thấy một sự chuyển mình bền vững trong hiệu quả R&D vẫn còn rất xa vời.
——————————————————————————–
Giới thiệu
Vấn đề năng suất trong nghiên cứu và phát triển (R&D) dược sinh học đã được mổ xẻ và thảo luận trong nhiều nghiên cứu khác nhau qua các năm. Là lĩnh vực thâm dụng nghiên cứu nhất, ngành dược sinh học chi hàng tỷ USD vào việc phát triển các liệu pháp điều trị mới với tốc độ tăng trưởng liên tục. Trong 70 năm qua, năng suất R&D (được định nghĩa là số lượng thuốc mới được phê duyệt mỗi năm) tương đối dậm chân tại chỗ, trong khi chi phí cho mỗi loại thuốc mới bắt đầu tăng vọt từ năm 1970. Chi phí trung bình để phát triển một loại thuốc mới đã tăng từ mức dưới 1 tỷ USD vào những năm 1990 lên 3,5 tỷ USD hiện nay.
Sự đột phá khoa học của công nghệ DNA tái tổ hợp vào những năm 1970, cùng với sự phát triển sau đó của các sản phẩm sinh học mới – như protein tái tổ hợp vào những năm 1980 và kháng thể đơn dòng vào những năm 1990 – đã tạo ra kỳ vọng lớn rằng những đổi mới trong công nghệ sinh học sẽ đẩy lùi sự suy giảm năng suất dược phẩm. Tuy nhiên, đến những năm 2010, chúng ta bắt đầu nhận ra rằng dù công nghệ DNA tái tổ hợp đã tạo ra nhiều liệu pháp sinh học đáng chú ý, dữ liệu thực tế lại không ủng hộ kỳ vọng rằng đổi mới công nghệ sinh học sẽ vực dậy năng suất R&D dược phẩm. Thay vào đó, hiệu quả R&D (được định nghĩa là số lượng thuốc mới được phê duyệt trên mỗi đô la Mỹ chi cho R&D) vẫn tiếp tục suy giảm đều đặn.
Các làn sóng đổi mới công nghệ sinh học gần đây hơn, bao gồm liệu pháp gen và tế bào cùng các sản phẩm y tế trị liệu tiên tiến (ATMPs) khác, có tiềm năng đảo ngược sự suy giảm năng suất này. Tuy nhiên, vì các làn sóng đổi mới trước đó đã thất bại trong việc phá vỡ xu hướng suy giảm, nên khả năng đảo ngược hiện tại vẫn chưa thực sự rõ ràng. Cho đến nay, hơn mười liệu pháp gen và tế bào đã được phê duyệt kể từ sau sản phẩm Provenge. Những loại ATMP này sử dụng các nền tảng khoa học phức tạp, không dễ dàng tích hợp vào mô hình kinh doanh R&D dược phẩm truyền thống vốn dành cho thuốc phân tử nhỏ hay các thuốc sinh học trước đây. Do đó, chúng chủ yếu tập trung vào các nhu cầu điều trị chưa được đáp ứng (unmet needs) và các bệnh hiếm (orphan diseases). Tuy nhiên, vì chúng ta mới chỉ bắt đầu khai phá tiềm năng của các phương pháp này, nên có lẽ còn quá sớm để đánh giá đầy đủ tác động của chúng đối với toàn ngành R&D dược phẩm.
Dữ liệu gần đây gợi mở về một sự xoay chuyển trong năng suất và hiệu quả R&D dược phẩm, nhờ vào những tiến bộ trong kiến thức di truyền học, hiểu biết sâu sắc hơn về bệnh lý, việc ra quyết định R&D được cải thiện và các rào cản pháp lý thấp hơn. Các chiến lược khác được các doanh nghiệp áp dụng bao gồm: tham gia vào các liên minh nghiên cứu và đối tác công – tư, tận dụng đổi mới mở (open innovation), và dựa vào các hoạt động đổi mới mang tính khám phá của các công ty công nghệ sinh học quy mô nhỏ và linh hoạt hơn. Chiến lược sau cùng đang được thực hiện ngày càng nhiều thông qua việc xây dựng mạng lưới các vườn ươm khởi nghiệp do các tập đoàn dược phẩm lớn hậu thuẫn như Bayer’s CoLaborator, J&J’s JLABS hay AstraZeneca’s BioVentureHubs.
——————————————————————————–
Khoảng cách năng suất dược phẩm và Hiệu quả R&D
Phân tích của chúng tôi cho thấy tốc độ mở rộng của khoảng cách năng suất dược phẩm đang chậm lại (Hình 1). Tốc độ tăng trưởng hàng năm kép (CAGR) trong 30 năm (1994–2023) là 6,5%, trong khi CAGR của 10 năm gần đây (2014–2023) chỉ còn 3,6%.
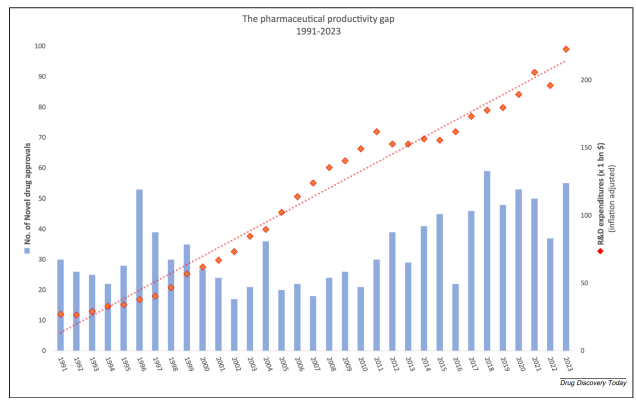
Khoảng cách năng suất trong ngành dược phẩm. Chi phí nghiên cứu và phát triển tăng đều đặn so với xu hướng trì trệ trong việc giới thiệu thuốc mới
Điều thú vị là số lượng thuốc mới được sản xuất mỗi năm đã tăng lên trong thập kỷ qua, với mức trung bình là 44 loại thuốc/năm, so với mức trung bình 34 của cả giai đoạn 30 năm qua. Chi phí phát triển một loại thuốc mới đã tăng từ mức trung bình động 3 năm là 0,86 tỷ USD năm 1999 lên 3,7 tỷ USD vào năm 2023. Tuy nhiên, mức chi phí trung bình trong 10 năm qua là 3,73 tỷ USD, phản ánh một xu hướng ổn định về hiệu quả. Tốc độ suy giảm dường như đang chậm lại trong khi cường độ R&D (chi phí R&D trên tổng doanh thu) vẫn duy trì ổn định ở mức khoảng 15%.
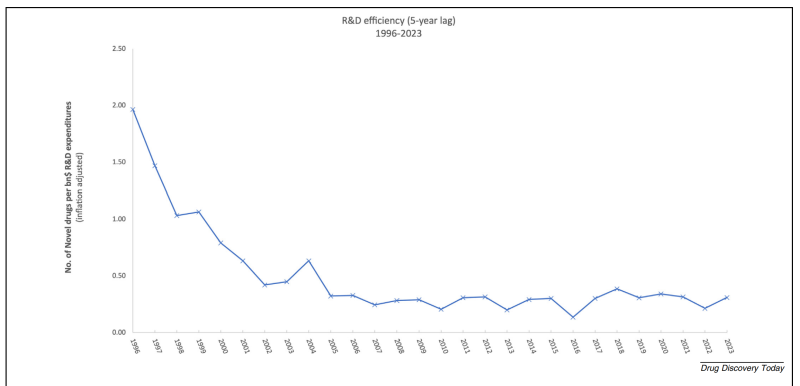
Hiệu quả nghiên cứu và phát triển, được thể hiện bằng số lượng thuốc mới được đưa ra thị trường trên mỗi 1 tỷ đô la chi phí nghiên cứu và phát triển trong 5 năm trước đó – đã điều chỉnh theo lạm phát (tính theo đô la Mỹ năm 2023).
Sự chậm lại của tốc độ suy giảm này có thể bắt nguồn từ các cải tiến quy trình nhằm nâng cao hiệu quả ở các giai đoạn phát triển thuốc khác nhau, từ đột phá trong hệ gen/hệ protein, hóa/sinh tin học cho đến các tiến bộ gần đây trong phân tích dữ liệu lớn (big data) và trí tuệ nhân tạo (AI). Ngoài ra, việc áp dụng đổi mới mở cho phép các công ty tích hợp công nghệ từ bên ngoài để giải quyết sự kém hiệu quả trong nội bộ. Tuy nhiên, phân tích của chúng tôi cho thấy những cải thiện này chỉ làm chậm lại chứ không làm đảo ngược xu hướng suy giảm dần vốn có.
——————————————————————————–
Sự hao hụt lâm sàng (Clinical Attrition)
Sự suy giảm dần năng suất R&D dường như phần lớn do tỷ lệ hao hụt lâm sàng ở giai đoạn muộn ngày càng tăng. Phân tích 81.532 thử nghiệm thuốc có can thiệp từ năm 2012 đến 2019 cho thấy xác suất thành công trung bình là 64% cho Giai đoạn I, 39% cho Giai đoạn II và 49% cho Giai đoạn III.
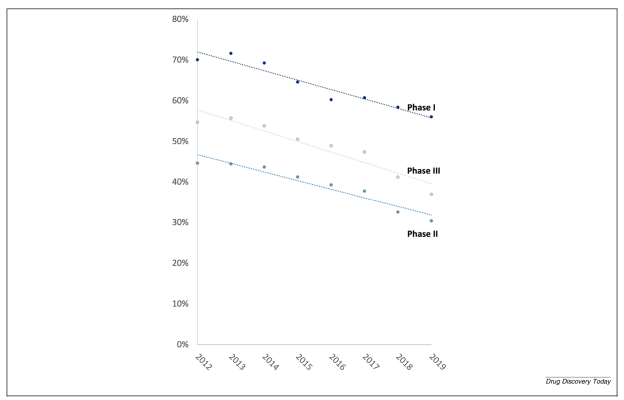
Xu hướng thành công của thử nghiệm lâm sàng theo từng giai đoạn (trong vòng 4 năm, đối với các thử nghiệm bắt đầu từ năm 2012 đến năm 2019). Tất cả các giai đoạn thử nghiệm lâm sàng đều cho thấy tỷ lệ bỏ cuộc ngày càng tăng qua các năm.
Đáng chú ý, mặc dù Giai đoạn II có tỷ lệ thất bại cao nhất, nhưng chính Giai đoạn III lại cho thấy sự gia tăng đáng kể của tỷ lệ hao hụt theo thời gian (Hình 3). Sự hao hụt ở giai đoạn sớm (Giai đoạn I) có thể coi là hiệu quả vì nó giúp loại bỏ các ứng viên kém tiềm năng trước khi đầu tư quá nhiều nguồn lực. Ngược lại, sự gia tăng thất bại ở Giai đoạn III – nơi các nguồn lực khổng lồ đã được đổ vào – là một vấn đề nghiêm trọng, phản ánh sự kém hiệu quả trong các giai đoạn sau của quá trình phát triển thuốc.
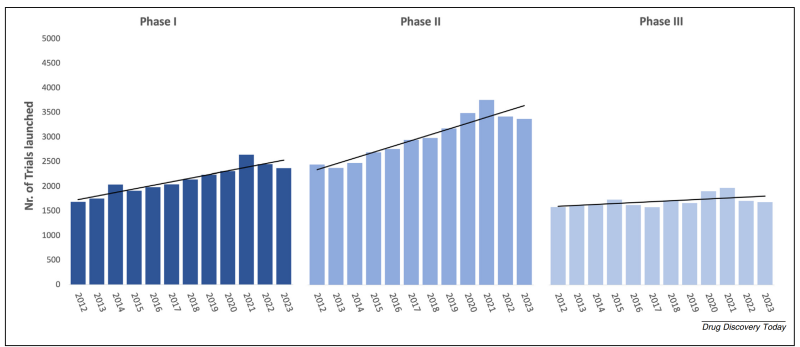
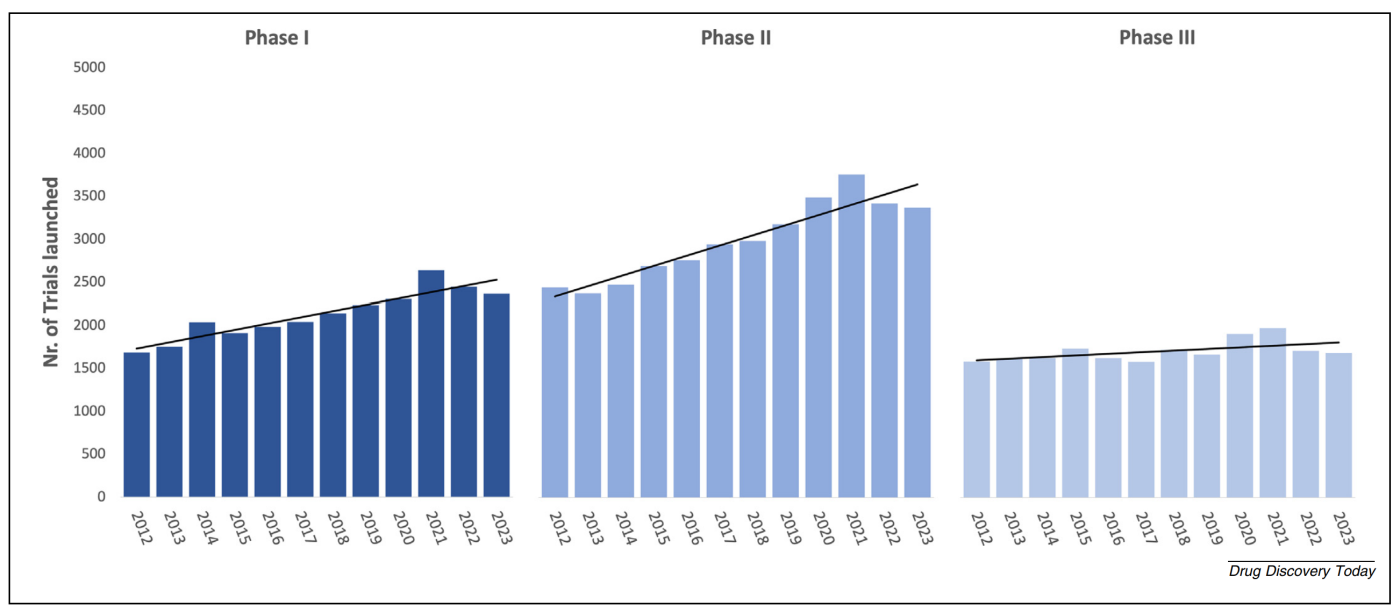
Số lượng thử nghiệm lâm sàng mới được khởi động hàng năm theo từng giai đoạn. Hình này minh họa xu hướng các thử nghiệm lâm sàng mới được khởi động mỗi năm, được phân chia theo giai đoạn thử nghiệm (Giai đoạn I,
Giai đoạn II, Giai đoạn III). Dữ liệu cho thấy sự khác biệt trong việc khởi động thử nghiệm ở các giai đoạn nghiên cứu lâm sàng khác nhau từ năm 2012 đến năm 2023.
Giai đoạn II, Giai đoạn III). Dữ liệu cho thấy sự khác biệt trong việc khởi động thử nghiệm ở các giai đoạn nghiên cứu lâm sàng khác nhau từ năm 2012 đến năm 2023.
Số lượng thử nghiệm lâm sàng mới bắt đầu cho Giai đoạn I và II tăng lên, nhưng Giai đoạn III vẫn dậm chân tại chỗ từ năm 2012–2023 (Hình 4). Điều này tạo nên một “nút thắt cổ chai” nghiêm trọng. Nghịch lý giữa tỷ lệ hao hụt Giai đoạn III tăng cao và sự ổn định của năng suất gần đây có thể phản ánh những cải thiện trong việc ra quyết định của các nhà quản lý, tập trung vào các dự án “rủi ro cao – lợi nhuận lớn”.
——————————————————————————–
Tính đại diện và Hạn chế
Nghiên cứu của chúng tôi tập trung vào 200 công ty dược sinh học lớn nhất, vì vậy kết quả có thể chủ yếu áp dụng cho các doanh nghiệp có quy mô tương đương. Việc tính toán hiệu quả R&D dựa trên độ trễ 5 năm (khoảng thời gian từ lúc đầu tư đến khi thuốc được phê duyệt) theo phương pháp của DiMasi et al. Chúng tôi thừa nhận rằng không phải toàn bộ chi phí R&D đều dành cho thuốc mới (mà còn dành cho công nghệ số, bảo hộ bằng sáng chế, quản lý liên minh), nên việc tính toán có thể chưa hoàn mỹ, nhưng kết quả vẫn nhất quán với các tài liệu hiện có.
——————————————————————————–
Nhận xét kết luận và Triển vọng
Phân tích của chúng tôi cho thấy sự giảm tốc và ổn định trong xu hướng suy giảm hiệu quả R&D kéo dài nhiều thập kỷ, thường được gọi là Định luật Eroom. Tuy nhiên, khác với các báo cáo lạc quan gần đây, nghiên cứu này không ủng hộ một sự xoay chuyển bền vững trong năng suất R&D. Tỷ lệ hao hụt lâm sàng giai đoạn muộn tăng cao vẫn là rào cản dai dẳng trong việc đưa các ứng viên thuốc ra thị trường.
Để đảo ngược sự suy giảm này về mặt cấu trúc, ngành dược phẩm cần đánh giá lại các mô hình kinh doanh hiện tại. Trong hơn 70 năm, mô hình thống trị vẫn là tập trung vào phát triển các thuốc “bom tấn” (blockbuster) mang lại doanh thu hàng tỷ USD mỗi năm. Chúng tôi cho rằng ngành cần chuyển dịch sang một hướng tiếp cận mở rộng và có khả năng quy mô hơn, đa dạng hóa các sáng kiến R&D và mở rộng phạm vi của các dự án khám phá để giảm thiểu rủi ro. Việc thúc đẩy một hệ sinh thái chia sẻ rủi ro và tăng cường hợp tác xuyên ngành (đặc biệt là với giới học thuật và các doanh nghiệp khởi nghiệp) sẽ giúp ngành dược vượt qua giới hạn hiện tại, khai thác hiệu quả hơn các tiến bộ khoa học kỹ thuật trong bối cảnh phát triển thuốc ngày càng phức tạp.
Tham khảo: Kenneth D.S. Fernald, Philipp C. Förster, Eric Claassen, Linda H.M. van de Burgwal,
The pharmaceutical productivity gap – Incremental decline in R&D efficiency despite transient improvements,
Drug Discovery Today,Volume 29, Issue 11, 2024,104160, ISSN 1359-6446, https://doi.org/10.1016/j.drudis.2024.104160.
(https://www.sciencedirect.com/science/article/pii/S135964462400285X)
The pharmaceutical productivity gap – Incremental decline in R&D efficiency despite transient improvements,
Drug Discovery Today,Volume 29, Issue 11, 2024,104160, ISSN 1359-6446, https://doi.org/10.1016/j.drudis.2024.104160.
(https://www.sciencedirect.com/science/article/pii/S135964462400285X)